
게티이미지뱅크 제공
지금으로부터 꼭 100년 전인 1918년 이 무렵, 일제 치하의 한반도에 끔찍한 독감이 맹위를 떨쳤다. 1918~19년 겨울을 나면서 인구의 절반인 740만 명이 감염돼 14만 명이 사망했다. 훗날 무오년독감(戊午年毒感)으로 불린 이 대유행의 ‘본명’은 당시 세계를 휩쓸며 5000만 명의 목숨을 앗아간 스페인독감이다.
이런 것도 100주년이라고 올겨울 독감의 기세가 만만치 않다고 한다. 질병관리본부의 발표에 따르면 환자 발생 건수가 예년 같은 기간의 두 배 가까이 돼 2009년 신종플루 대유행 이후 가장 높다. 그나마 다행인 건 아직까지 독감 바이러스의 병원성이 평범하다는 것이다.
100년 전 스페인독감 때는 병원체의 실체조차 모르고 당했지만(1930년대 전자현미경이 발명되면서 바이러스가 모습을 드러냈다), 지금은 입자구조에 유전자에 속된 말로 독감 바이러스를 완전히 발가벗겨놨음에도 여전히 바이러스의 처분만 기다리고 있으니 어쩐 일일까.
물론 매년 늦가을 독감예방(백신)접종을 실시하지만, 겨울에 유행할 독감 바이러스에 효과가 있다고 보장할 수 없다는 게 문제다. 2009년 신종플루가 그런 경우로, 전염성이 큰 데다 병원성까지 심각할 것으로 보이는 바이러스를 기존 백신으로 잡지 못해 세계 보건계가 총출동해 부랴부랴 신종플루용 백신을 만들어 공급하던 모습이 생생하다.
이 모든 일들은 쉽게 돌연변이를 일으킬 수 있는 독감 바이러스의 특성에서 비롯된다. 백신에 들어있는 바이러스의 표면 단백질에 달라붙는 항체가 형성돼도 막상 유행하는 바이러스의 표면 단백질 구조가 꽤 다르면 인식하지 못하기 때문에 소용이 없다.
올해 유행하고 있는 독감 바이러스는 백신에서 예측한 범위에 들어있다고 하니 다행이지만 2009년 신종플루 같은 사태가 벌어진 개연성은 남아 있다.
그렇다면 우리는 언제까지 이처럼 효과가 확실하지도 않은 백신을 그것도 매년 맞아야 하는 걸까. 천연두나 소아마비 백신처럼 한두 번만 맞으면 어떤 독감 바이러스가 유행해도 면역력을 가질 수 있는 만능 독감 백신(universal flu vaccine)은 언제쯤 나올까.
만능 독감 백신, 여전히 희망사항
학술지 ‘사이언스’ 12월 7일자에는 만능 독감 백신이 ‘연금술사의 꿈’이라는 제목의 기사가 실렸다. 중세시대 연금술사들이 쇠를 금으로 바꾸는 꿈을 꾼 데 비유하고 있으니 만능 독감 백신 개발 전망을 짐작할 수 있을 것이다.
기사는 최근 비영리단체인 ‘인간 백신 프로젝트’ 주관으로 열린 바이러스 학자들의 모임 취재기인데, “매년 우리는 이 바이러스에 대해 아는 게 점점 적다는 걸 배울 뿐이다”라는 한탄에서 “1960년대 첫 모임을 가진 이래 여전히 동일한 문제에 봉착해 있다”는 토로까지 학자들의 좌절감이 느껴진다.
가장 큰 이유는 독감 바이러스가 변이를 거의 일으키지 않는 부분으로 백신을 만들면 이에 대한 항체가 형성되더라도 진짜 바이러스가 침투했을 때 제대로 작동하지 못한다는 데 있다. 예를 들어 독감 바이러스의 표면 단백질인 헤마글루티닌(hemagglutinin)은 버섯처럼 생겼는데, 변이가 없는 부분은 거의 줄기에 있다. 그런데 이를 인식하는 항체는 덩치 때문에 헤마글루티닌의 줄기에 접근하기 어렵다.
참고로 독감 바이러스로 만든 백신을 맞으면 형성되는 항체 대다수는 접근하기 쉬운 돌출된 부분(버섯의 갓에 해당)을 인식한다. 독감 바이러스는 당연히 이에 대응해 이 부분에 변이가 쉽게 생겨도 기능에 문제가 없게 진화한 것이다.
만능 독감 항체 등장
‘사이언스’ 11월 2일자에는 만능 독감 백신을 대신할 수 있는 만능 독감 항체를 만드는 데 성공했다는 연구결과가 실렸다. 미국 스크립스연구소가 주축이 된 다국적 연구팀은 나노항체 유전자 네 개를 이어 붙여 아데노바이러스-관련 바이러스(adenovirus–associated virus. 이하 AAV) 게놈에 넣었다.
그리고 AAV가 들어있는 스프레이를 코에 뿌려주면 나노항체 네 개로 이뤄진 단백질을 만들어 어떤 유형의 독감 바이러스가 침투하더라고 무찌를 수 있다는 걸 생쥐 동물실험으로 보여줬다. 만능 독감 백신의 꿈을 대신할 만능 독감 항체를 만드는 데 성공했다는 것이다.
이번 연구의 핵심인 나노항체(nanobody)부터 알아보자. 한 세대 전인 1980년대 후반 벨기에 자유대 연구자들은 동물기생충을 연구하기 위해 사람의 혈액을 분석하는 연구를 진행하고 있었다. 그런데 에이즈가 창궐하면서 감염 공포로 연구원들이 사람 혈액 분석을 피했고 대안인 생쥐를 죽이기도 거부했다. 결국 냉동 보관 중인 단봉낙타의 혈장(혈액의 액체 부분)을 이용하기로 했다.
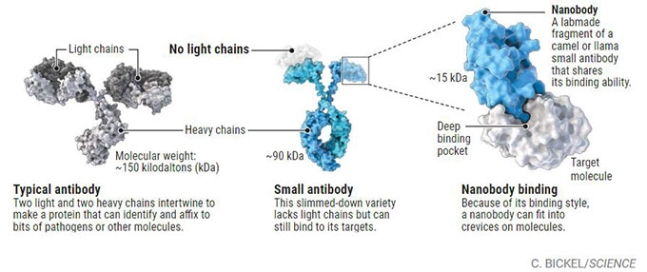
사람 면역계가 만드는 항체는 긴 사슬(옅은 회색) 두 개와 짧은 사슬(짙은 회색) 두 개로 이뤄져 있어 덩치가 크다(왼쪽). 반면 낙타과(科) 동물이나 상어는 긴 사슬 두 개로만 이뤄진 작은 항체를 만들 수 있다(가운데). 작은 항체에서 항원과 인식하는 부분에 해당하는 정보를 담은 DNA조각을 박테리아나 바이러스의 게놈에 넣어주면 나노항체를 만들 수 있다. 아래 흰 분자가 항원이다(오른쪽). ‘사이언스’ 제공
그런데 낙타 혈장에 전형적인 항체와 함께 특이한 항체가 존재한다는 사실이 밝혀졌다. 보통 항체는 Y자 모양으로 긴 사슬(heavy chain) 두 개와 짧은 사슬(light chain) 두 개로 이뤄져 있다. 그런데 낙타 혈장에는 긴 사슬 두 개로만 이뤄진 작은 항체가 존재했다. 긴 사슬만으로도 항원을 인식할 수 있는 항체다. 그 뒤 쌍봉낙타와 라마 등 낙타과(科) 동물과 상어의 혈장에 작은 항체가 존재한다는 사실이 밝혀졌다.
그 존재 이유는 여전히 미스터리이지만 분류학적으로 꽤 떨어져 있는 두 동물군에서 수렴진화로 나타났다는 사실은 작은 항체가 이들 동물의 생존에 꽤 중요함을 시사한다.
과학자들이 작은 항체에 주목한 건 덩치가 작기 때문에 기존 항체가 접근하기 어려운 부분을 항원으로 하는 항체도 만들어질 수 있기 때문이다. 예를 들어 독감 바이러스의 경우 헤마글루티닌 줄기의 변이가 잘 일어나지 않는 부위를 항원으로 하는 작은 항체가 생성될 수 있다.
게다가 작은 항체에서 항원을 인식하는 부분만 따로 떼어내 대량으로 만들 수 있다는 것도 큰 장점이다. 항원과 결합한 상태에서 작은 항체의 구조를 분석한 뒤 인식하는 부분의 아미노산 서열을 읽으면 여기에 해당하는 DNA서열을 알 수 있다. 이 DNA 조각을 박테리아나 바이러스의 게놈에 넣으면 이들이 항원을 인식하는 부분인 작은 단백질인 나노항체를 만든다.
나노항체 네 개 조합해 효과 극대화
연구자들은 라마에 독감 바이러스 세 종과 헤마글루티닌 단백질 두 종으로 이뤄진 백신을 주사한 뒤 혈장을 채취해 형성된 작은 항체들을 분석했다. 그 결과 A형 독감 바이러스의 헤마글루티닌 줄기를 항원으로 하는 작은 항체 두 종을 골라 각각의 나노항체 부분을 규명했다(SD36과 SD38). 그리고 B형 독감 바이러스의 헤마글루티닌 줄기와 갓임에도 변이가 적은 부분을 항원으로 하는 작은 항체 두 종을 골라 각각의 나노항체 부분을 규명했다(SD83과 SD84).

독감 바이러스 3종과 헤마글루티닌(HA) 단백질 2종으로 만든 백신을 라마에 접종해 유도한 항체들에서 헤마글루티닌 불변 영역을 항원으로 하는 작은 항체 네 가지를 선별했다. 이 가운데 두 가지는 A형 독감 바이러스의 헤마글루티닌 단백질의 줄기 부분에 달라붙고(왼쪽) 나머지 두 가지는 B형 독감 바이러스의 헤마글루티닌 단백질의 줄기와 갓에 각각 달라붙는다(가운데). 연구자들은 이 네 가지 작은 항체에서 얻은 나노항체의 유전자를 연결해 모든 유형의 독감 바이러스를 인식할 수 있는 조합항체를 만들었다(오른쪽). ‘네이처’ 제공
연구자들은 이들 나노항체 네 가지의 유전자를 연결해 만든 조합항체 MD3603의 유전자를 아데노바이러스-관련 바이러스(AAV)의 게놈에 넣었다. AAV는 인체 세포에 침투해 일정 기간 증식하지만 인체에 무해해 유전자 치료 실험에 즐겨 쓰는 바이러스다.
조합항체 MD3603의 효과를 알아보기 위해 AAV를 넣은 스프레이를 다양한 독감 바이러스에 감염시킨 생쥐의 코에 뿌려 생존율을 조사했다. 그 결과 보통 1주일이면 모두 죽는 병원성이 큰 독감 바이러스에 대해서도 대부분 살아남았다. 헤마글루티닌의 서로 다른 불변 영역을 인식하는 항체가 네 가지나 되다 보니 A형과 B형 가리지 않고 테스트한 모든 독감 바이러스를 항원으로 인식할 수 있었다.
연구자들은 조합항체 MD3603이 면역력이 약해 독감 백신을 맞아도 항체가 잘 형성되지 않는 고령층에 특히 유용할 것으로 내다봤다. 예방접종주사를 맞을 때 코에 MD3603 AAV 스프레이를 뿌려주면 비강의 세포에 침투한 AAV가 겨울 한 철 동안 조합항체를 생산해 독감 바이러스가 들어와도 바로 퇴치하기 때문이다. AAV가 사람의 면역세포를 대신해 더 효과적인 항체를 만드는 셈이다.
물론 이 기술이 사람에 적용될 때까지는 갈 길이 멀다. AAV가 안전하다고는 해도 아직 보편적으로 쓰일 만큼 신뢰를 얻은 건 아니기 때문이다. 게다가 인체의 면역계가 조합항체를 항원으로 인식해 이에 대한 항체를 만들 수도 있다. 그럼에도 만능 독감 백신 개발이 요원한 상태에서 대안이 될 수 있는 이번 연구결과에 많은 바이러스 학자들이 찬사를 보내고 있다.
메르스(중동호흡기증후군) 바이러스의 매개체로 이미지를 구긴 낙타가 인류를 독감에서 구해낼지 지켜볼 일이다.
(원문: 여기를 클릭하세요~)