英서 ‘유전자가위’ 실험 성공
유전자 편집기술로 불임 유도
야생모기와 교미 시킬 경우
몇 세대 걸치면 종 완전 박멸
모기는 사람 피를 빨아먹고 말라리아 황열 뇌염 등 치명적 질병을 일으킨다. 성가실 뿐만 아니라 백해무익하기에 모두 없애버리는 게 낫다고 여기는 사람이 많다. 실제로 유전공학을 이용해 모기 박멸 가능성을 확인한 과학자들이 있다.
21일 한국생명공학연구원에 따르면 영국 런던 임페리얼칼리지 생명과학부 연구팀은 말라리아를 퍼뜨리는 모기의 불임을 유도하고, 불임 모기와의 세대별 교미를 통해 모기를 박멸시켰다는 논문을 지난해 11월 ‘네이처바이오테크놀로지’에 실었다. 임페리얼칼리지 연구진은 모기 불임을 유도할 때 3세대 유전자가위 ‘크리스퍼(CRISPR)-카스(CAS)9’을 썼다. 생식능력을 부여하는 특정 유전물질을 이 유전자가위로 잘라버린 것이다.
최근 국내에서도 유전자가위에 대한 관심이 높아지고 있다. 국내 독보적인 크리스퍼-카스9 기술을 갖고 있는 코넥스 상장업체 툴젠이 지난 19일 바이오업체인 제넥신에 흡수합병됐다. 툴젠은 유전자가위 분야 국내 최고 권위자인 김진수 전 서울대 교수의 기술을 이전받은 업체다.
Getty Images Bank
DNA 일부 ‘싹둑’ 잘라
유전자가위는 DNA 특정 부위를 자르는 일종의 ‘유전자 편집’ 기술이다. 1953년 DNA의 이중나선구조 발견 이후 유전자 재조합, 유전자 서열 분석 및 증폭, 인간게놈 프로젝트 등으로 이어진 바이오공학 가운데서 최신 기술로 평가받는다. 구체적으로 보면 DNA의 30억 염기쌍 가운데 일부(타깃)를 절단해 형질을 바꾼다.
2000년대 처음 등장한 1세대 유전자가위는 ‘ZFN’이다. 타깃으로 안내하는 ‘아연집게 단백질’에 가위 역할을 하는 핵산분해효소(뉴클레아제)를 결합해 만들었다. 2세대인 ‘탈렌’을 넘어 현재 각광받고 있는 것은 3세대 유전자가위 크리스퍼-카스9이다. 세대가 높아질수록 자르는 효율과 정교함이 높아진다.
크리스퍼-카스9은 가위 역할을 하는 단백질 ‘카스9’에 ‘가이드RNA’를 붙인 것이다. RNA는 DNA의 다양한 복사본인데, 가이드RNA는 ‘정밀유도시스템’과 같이 카스9이 어디를 자를지 안내해준다. 카스 단백질은 카스9, 카스12, 카스13, 카스14 등 여러 가지가 있다. 카스 종류에 따라 가이드RNA 성질을 바꿔야 하고, 이에 따라 자를 수 있는 유전자 타깃도 달라진다. 크리스퍼는 ‘앞뒤 서열이 같은 유전물질 군집체(clusteredregularly interspaced short palindromic repeats)’의 줄임말이다.
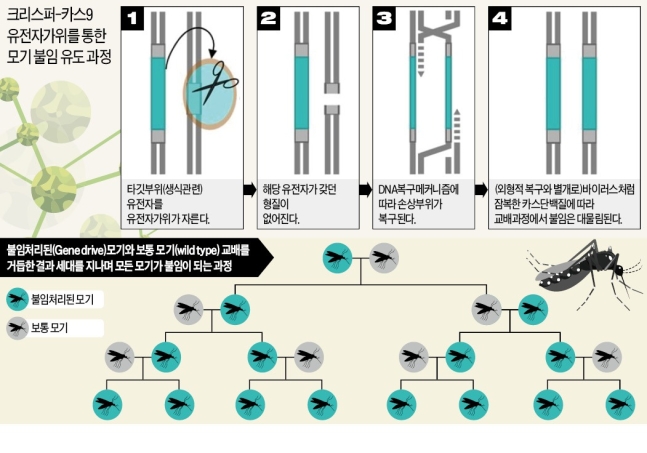
3세대 유전자가위로 모기 박멸
영국 임페리얼칼리지 연구팀은 300마리의 정상 암컷 모기와 150마리의 정상 수컷 모기, 그리고 크리스퍼-카스9 유전자로 불임처리한 암컷 모기 150마리를 폐쇄된 공간에 넣고 세대를 거쳐 연구를 했다. 자식은 부계, 모계로부터 각각 유전자를 받기 때문에 불임처리된 암컷 모기와 정상 수컷 모기 사이 태어난 모기는 불임이 된다.
연구팀은 여러 조건에서 확인 결과 7~11세대가 지나면 600마리로부터 시작된 ‘모기 가계’가 모두 멸종하는 것을 확인했다고 논문에서 밝혔다. 특정 시점이 되면 모두 불임이 되면서 후손 생성이 중단된 것이다.
통제된 실험실이 아니라 자연환경에서도 ‘불임 공학’을 통한 박멸이 가능할지는 미지수다. 내성을 가진 개체가 등장하는 등 변수가 많기 때문이다.
김용삼 한국생명공학연구원 유전자교정연구센터장은 “크리스퍼-카스9 유전자가위로 불임을 만들면 해당 자손은 이론적으로 모두 불임이 된다”며 “특정 종을 말살시킬 ‘바이오 무기’로 활용될 수 있기 때문에 생명윤리상 큰 이슈”라고 말했다.

김용삼 한국생명공학연구원 유전자교정연구센터장(왼쪽)이 연구원들과 실험 결과를 토론하고 있다. 한국생명공학연구원 제공
기술적 한계 극복해야
세계보건기구(WHO)에 따르면 2016년 전 세계에서 말라리아로 44만여 명이 목숨을 잃었다. 공식적으로 ‘인간을 가장 많이 죽인 동물(곤충)’이 모기다. 모기 박멸은 인간에겐 축복이 될 수 있지만 자연 생태계 교란 가능성이 크다는 점이 문제로 지적되고 있다. 모기를 먹이로 하는 여러 생물에 예상치 못한 영향을 줄 수 있기 때문이다.
유전자가위는 무궁무진한 가능성이 있다고 평가받는다. 조류인플루엔자(AI) 등 여러 질병에 저항성을 갖는 가축이나 특정 기능성을 증폭시킨 슈퍼작물(GMO)을 만들 수도 있다. 인간의 경우 질병 가족력이 있다면 해당 타깃을 잘라 후대로의 열성 형질 대물림을 차단할 수도 있다. 마켓리서치엔진에 따르면 크리스퍼 유전자가위 세계시장 규모는 지난해 7600억원에서 2022년 2조6700억원으로 증가할 전망이다.
아직 기술적으로 넘어야 할 과제는 많다. 먼저 타깃 유전자가 제대로 잘라지는지가 변수다. 특정 유전자가 절단될 경우 의도치 않게 다른 엉뚱한 유전자 변형이 일어날 가능성도 배제할 수 없다. 돼지열병 등을 막으려다 다른 질병에 취약해질 수도 있다는 얘기다.
(원문: 여기를 클릭하세요~)
Researchers combined sterilization with a bacterium in an attempt to stamp out the Asian tiger mosquito.
Asian tiger mosquitoes bite during the day and can transmit diseases including chikungunya.Credit: Gordon Zammit/Alamy
Researchers have all but obliterated populations of the world’s most invasive mosquito species — the Asian tiger mosquito (Aedes albopictus) — on two islands in the Chinese city of Guangzhou.
They reduced A. albopictus populations by up to 94% using a combination of two promising control techniques in a field trial for the first time. The two-pronged approach1, published in Nature on 17 July, integrates the sterilization of female Asian tiger mosquitoes with the infection of males using Wolbachia pipientis, a bacterium that hinders the insects’ ability to reproduce and transmit disease-causing viruses such as dengue and Zika.
This resulted in one of the most successful eradication trials of A. albopictus to date, says Peter Armbruster, a mosquito ecologist at Georgetown University in Washington DC, who wrote a commentary to accompany the study. Used in tandem with other control methods such as pesticides, the dual approach could be a very powerful tool, he says.
Problems with control
Previous studies have shown that X-ray sterilization of large numbers of male pests like screw worms (Cochliomyia hominivorax), followed by their release into target areas, can reduce the size of wild pest populations. But this is an inefficient way to control mosquitoes because even though irradiated males can still mate, they are less successful than their unaltered counterparts.
In an alternative approach, workers infect laboratory mosquitoes with strains of Wolbachia, which is found naturally in several insect species, including A. albopictus. When male mosquitoes infected with a certain combination of Wolbachia strains mate with wild females carrying a different combination, the insects can’t produce offspring.
But it’s crucial that only male mosquitoes infected with that particular combination are released into the wild, says Zhiyong Xi, a medical entomologist at Michigan State University in East Lansing, who led the study. If females with those strains are also released, they could mate and produce offspring with males carrying the same Wolbachia cocktail. Their offspring could eventually replace the local mosquito population, making future control attempts that rely on Wolbachia infection more difficult.
To prevent this from happening, facilities that rear large numbers of mosquitoes for control purposes usually separate males from females mechanically, based on size differences. But this process isn’t perfect, Xi says, so workers have to do a second, manual screening to remove female mosquitoes. It’s a tedious and time-consuming task that limits the total number of mosquitoes that can be released. So Xi and his team set out to eliminate the need for this process.
An issue of scale
Wild populations of A. albopictus are naturally infected with two strains of Wolbachia. The researchers infected wild mosquitoes with a third strain of Wolbachia to produce a laboratory colony of the insects with three bacterial variants. Then, the team exposed the colony to low levels of radiation that sterilized the females but only slightly reduced the males’ ability to mate.
During the mosquitoes’ peak breeding seasons in 2016 and 2017, the researchers released more than 160,000 of these mosquitoes per hectare each week in residential areas on two islands situated in a river in Guangzhou — the city with the highest rate of dengue transmission in China.
Their hope was that this would vastly reduce the mosquito population because wild females that mated with the altered males — and wild males that mated with sterile lab females — wouldn’t produce offspring. The team tracked population declines in adult female mosquitoes, since they’re the ones that bite people and transmit diseases. And as expected, the average numbers of wild adult females fell by 83% in 2016 and by 94% in 2017.
Male Asian tiger mosquitoes carrying three strains of Wolbachia await release into a test site.Credit: Yajun Wang
“That’s very impressive,” says Stephen Dobson, a medical entomologist at the University of Kentucky in Lexington, and the founder of MosquitoMate, a company that commercializes Wolbachia as a tool to control the Asian tiger mosquito.
Current strategies for controlling A. albopictus — including spraying pesticides and removing water-filled containers where the insects lay their eggs — are ineffective, Dobson says. This species lays its eggs in hidden places that can be difficult to monitor and tends to develop resistance to common insecticides, he adds. “A new tool like what’s being described in this paper is very much needed,” he says.
But scaling up the technique into an effective public-health strategy for large regions is the challenge, says Gordana Rašić, a molecular ecologist at the QIMR Berghofer Medical Research Institute in Brisbane, Australia.
Rašić says that Wolbachia-based approaches are promising strategies, and she’s hopeful that developing and testing such tools will help to reduce the incidence of mosquito-borne diseases. “We’re living in very exciting times for mosquito control,” she says.
(원문: 여기를 클릭하세요~)
중국 ‘모기와의 전쟁’ 성과
흰줄숲모기 수컷 생식력 감소 위해
방사선 쪼이고 세균까지 감염시켜
알 낳아도 부화 못하거나 수명 짧아
모기 개체 수 매년 83~94%씩 줄어
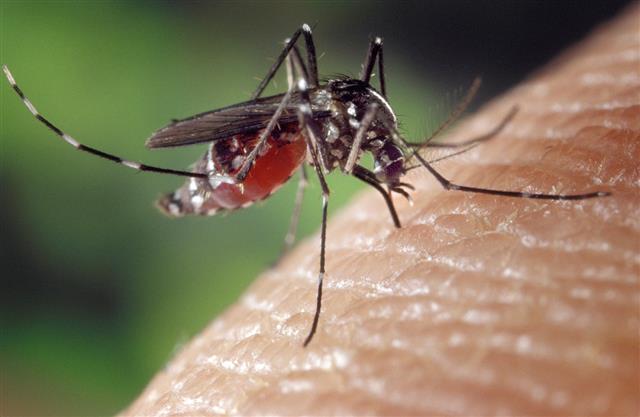
픽사베이 제공
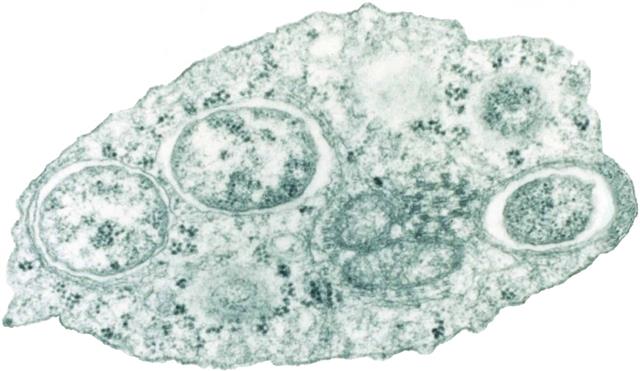
세균 ‘볼바키아’.위피피디아 제공
평년 기준으로 올해 장마도 일주일 정도 뒤면 끝날 것이다. 장마가 막바지에 다다르면서 날씨도 점점 더워지고 있다. 여름밤 무더위에 지쳐 까무룩 잠에 들라치면 갑자기 귓가에서 ‘애앵’ 소리를 내면서 꿀잠을 방해하는 골칫거리도 기승을 부릴 것이다. 바로 여름밤의 불청객 ‘모기’이다.
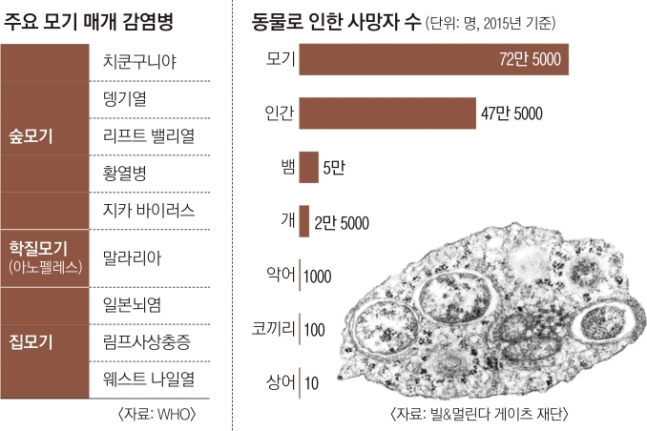
●“매년 7억명 이상 모기 인한 전염병 걸려”
모기는 일본뇌염, 말라리아뿐만 아니라 뎅기열, 황열병, 웨스트나일 바이러스, 지카 바이러스 등 치명적인 감염병을 옮겨 인류의 건강을 위협하는 해충이다. 실제로 세계보건기구(WHO)에 따르면 매년 7억명 이상의 사람이 모기로 인한 전염병에 걸리고 이 중 100만명이 사망한다.
모기가 시각적으로 사람을 알아보고 피를 빠는 것으로 생각하지만 그렇지 않다. 일반적으로 사람은 피부를 통해 350여 가지 화합물을 배출하는 것으로 알려져 있다. 모기는 이 중 호흡을 통해 배출되는 이산화탄소, 땀 속에 포함된 1-옥텐-3올, 락트산 같은 화합물과 체열에 이끌린다. 모기는 머리에 있는 깃털처럼 생긴 더듬이와 턱 쪽에 있는 짧은 더듬이에 후각 신경세포를 갖고 있다. 짧은 더듬이는 30m나 떨어져 있는 사람의 숨 속에 포함된 이산화탄소를 감지할 정도로 민감하게 작동한다.
밤잠을 설치게 만들고 각종 질병을 옮기는 모기를 박멸하기 위해 과학자들은 다양한 방법을 연구해 왔다. 천적을 이용한 고전적인 퇴치법에서부터 유전자를 변형시킨 GM모기나 방사선, 박테리아로 불임 모기를 만드는 방법까지 등장하고 있다.
방사선을 쬐어 생식능력을 떨어뜨린 수컷 모기들은 일반 수컷 모기들에 비해 번식 경쟁력이 지나치게 떨어진다는 문제가 있었고 세균을 이용하는 방법은 실험실 수준에 그쳐 효과가 확실하지 않았다.
●“지금까지 나온 모기 퇴치법 중 가장 효과적”
이 같은 상황에서 중국 중산대·미국 미시간주립대 열대병요인통제 통합연구센터, 국제식량농업기구(FAO)·국제원자력기구 공동 해충통제연구소, 호주 멜버른대 생명과학부 바이오21연구소와 9개 중국 대학 및 연구기관이 참여한 공동연구팀은 방사선 기술과 모기의 생식력을 감소시키는 세균을 함께 사용해 모기를 거의 완벽하게 퇴치하는 데 성공했다. 이 같은 연구결과는 세계적인 과학저널 ‘네이처’ 18일자에 실렸다.
연구팀은 한국과 일본, 중국을 비롯해 호주, 유럽 등 거의 전 세계에 서식하면서 각종 전염병을 옮기는 흰줄숲모기(Aedes albopictus)를 대상으로 실험을 했다.
연구팀은 방사선으로 수컷 모기의 생식 능력을 적정 수준까지 떨어뜨리고 ‘볼바키아’(Wolbachia)라는 세균에 감염시키는 이중 처리를 한 다음 야생에 방사했다. 볼바키아는 곤충의 세포 속에서 기생하면서 곤충의 생식 능력을 떨어뜨리는 세균으로 알려져 있다. 실제로 볼바키아에 감염된 수컷 모기의 자손들은 알에서 부화하지 못하거나 태어나자마자 죽거나 수명이 짧아진다.
연구팀은 중국 광저우시 일부 지역에 방사선을 쬐고 볼바키아로 감염시킨 수컷 모기를 방사한 뒤 2년 동안 추적조사한 결과 모기의 개체수가 매년 83~94%씩 줄어들면서 야생 모기 대부분이 제거됐다고 밝혔다. 현재 해당 지역에서 발견되는 모기들은 실험 지역 바깥에서 유입된 것으로 인구유전학적 분석결과 확인됐다.
이번 연구를 주도한 시지용 미국 미시간주립대 교수(미생물학·분자유전학)는 “이번 연구는 지금까지 나온 모기 퇴치 방법 중 가장 효과적인 것으로 모기로 인한 각종 전염병에서 인류를 구해 줄 수 있을 것”이라고 말했다.
(원문: 여기를 클릭하세요~)
브라질 뎅기열 모기 박멸사업 효과 논란…연구진·개발사 충돌
‘유전자 바뀌치기 모기 죽지 않고 번식’ vs ‘사실무근’ 반박
뎅기열과 지카바이러스 등을 옮기는 모기를 유전자 바꿔치기 기술로 박멸하는 실험은 실패로 끝난 걸까.
브라질 현지를 조사한 미국과 브라질 연구팀이 “야생 모기와 교배해 태어난 유충은 (개발업체 주장대로) 사멸해야 하는데도 번식하는 것으로 확인됐다”는 논문을 발표하자 유전자 바꿔치기 모기를 개발한 바이오회사가 ‘사실 무근’이라며 강력하게 항의, 양측의 주장이 정면으로 충돌하고 있다.
논쟁의 발단은 영국 바이오기업 ‘옥시테크’가 브라질 동부 도시 자코비나에서 2013~2015년 유전자를 바꿔친 열대숲모기 수컷을 매주 45만 마리씩 방사한 실험이다. 이 수컷 모기와 야생 암컷 모기가 교배해 태어난 유충은 성충이 되기 전에 죽는 것으로 돼 있다. 이대로만 되면 살충제처럼 생태계에 큰 부담을 주는 방법을 쓰지 않고도 모기를 줄일 수 있을 것으로 생각됐다.

그러나 미국 예일대학과 브라질 연구팀은 지난 9월 “일시적으로 모기가 줄기는 했지만 1년 반후 다시 원래 상태로 돌아갔다”며 효과에 의문을 제기하는 논문을 영국 과학지 사이언티픽 리포트에 발표했다.
논문에 따르면 야생 모기에서 유전자를 바꿔친 모기의 DNA 일부가 검출된 사례도 있다. 죽지 않고 성충이 된 모기가 어느 정도 있었던 것으로 보인다.
연구팀은 유전자를 바꿔친 모기는 쿠바와 멕시코 모기를 교배시켜 만든 것이어서 “성충이 된 모기는 유전적으로 다양해져 번식력이 오히려 강해졌을지도 모른다”고 우려를 표명했다.
옥시테크사는 자사 사이트에 “모기 수가 원래대로 돌아간 건 실험이 끝난 후”라고 지적하고 “살아남은 모기가 3~5% 있지만 거의 다 죽기 때문에 최종적으로는 숫자가 줄어든다”고 반박했다.
또 “안전성을 보고한 100편 이상의 연구성과를 의도적으로 무시하고 드라마틱한 논평으로 사실무근의 불안감을 조성했다”고 비판했다.
항의를 받은 출판사 측은 온라인판 논문(https://doi.org/10.1038/s41598-019-49660-6)에서 향후 대책을 검토하고 있다고 밝힌 것으로 아사히(朝日)신문이 10월 31일 전했다.
(원문: 여기를 클릭하세요~)
곤충학에 대해서 조금더 알아보고 싶으면, 여기를 클릭하세요~
(If you want to know more about entomology, please click here~)
“Entomology 101: Study Of Insects For Beginners [A Rare Guide]”
아래는 2022년 4월 26일 뉴스입니다~
(원문: 여기를 클릭하세요~)
유전자 조작 모기로 모기 없앤다…美 첫 실험 성공
날이 따뜻해지면서 여름의 불청객, 모기도 벌써 모습을 드러내고 있습니다.
미국에서 유전자 조작 모기를 이용해 야생의 모기 수를 줄이는 실험을 한 결과 성공적이었다는 소식이 전해졌습니다.
최소라 기자입니다.
[기자]
4∼7㎜의 몸통에 희고 검은 줄무늬가 있는 다리,
열대 지방 등에 서식하는 이집트숲모기입니다.
이집트숲모기 암컷은 알을 낳기 위해 사람 피를 빨아먹는데, 그 과정에서 뎅기열이나 지카 등 치명적인 바이러스를 전파합니다.
[라지브 바이디야나탄 / 모기 전문가 : 이집트숲모기는 식물에 숨어 살고, 알 까는 곳을 찾아내기 힘듭니다. 연구에 따르면 살충제에 대한 내성도 높습니다.]
과학자들이 유전자 편집 기술을 이용해 모기 박멸에 나섰습니다.
모기의 알에 바늘을 찔러 넣고 연구진이 만든 유전자 조각을 넣어줍니다.
이렇게 태어난 수컷 모기는 야생 암컷 모기와 짝짓기를 해 자손을 퍼트리는데, 이 가운데 암컷 자손은 유충일 때 죽어버리고, 사람 피를 빨지 않는 수컷 자손만 살아남는 겁니다.
연구팀은 지난해 미 플로리다주에 유전자 조작 모기 500만 마리를 풀어놓고 모기 서식지를 관찰했습니다.
일부 지역에선 유충이 확연히 줄었고, 채취된 유충 2만여 마리는 모두 조작된 유전자를 가지고 있었습니다.
이 가운데 암컷 유충은 성충이 되기 전에 모두 죽은 것으로 나타났습니다.
연구팀은 유전자 조작 동물에 대한 세간의 우려에 대해서, 이번 실험이 인간이나 생태계에 부작용을 일으킬 우려는 적다고 말했습니다.
[네이든 로즈 / 과학자 : (2∼3달 정도의) 시간이 지나면서 유전자 조작 모기가 자연에서 완전히 사라졌습니다. 이것은 조작된 유전자가 환경에 오랫동안 남아 있지 않다는 방증입니다.]
연구팀은 미 캘리포니아주에서도 모기 방사 실험을 진행할 예정입니다.
또 말라리아를 퍼트리는 모기를 대상으로도 유전자 조작 모기를 개발하겠다며, 아프리카와 중미에서 실험을 진행할 계획이라고 밝혔습니다.
연구팀은 이번 실험이 모기 매개 감염병 감소로까지 이어질지는 지켜봐야 하지만, 모기 수를 줄이는 데는 성공적이었다고 평가했습니다.

